Гиперкортицизм – это заболевание надпочечников, в результате которого значительно повышается уровень кортизола в организме. Эти глюкокортикоидные гормоны принимают непосредственное участие в регулировании обмена вещества и множества физиологических функций. Надпочечники контролируются гипофизом, посредством выработки адренокортикотропного гормона, который активизирует синтизацию кортизола и кортикостерона. Что происходит с людьми при данном синдроме, какие причины его возникновения и как лечить заболевания, мы рассмотрим далее в статье.

Гиперкортицизм: что это такое?
Гиперкортицизм или синдром Иценко-Кушинга, представляет собой эндокринную патологию, связанную с продолжительным и хроническим воздействием на организм избыточного количества кортизола. Такое воздействие может возникать вследствие имеющихся недугов или на фоне приема некоторых медикаментов. Женщины в 10 раз чаще мужчин страдают гиперкортицизмом, и, в основном, в возрасте от 25 до 40 лет.
Чтобы нормально функционировал гипофиз, необходима достаточная выработка конкретных гормонов гипоталамусом. Если нарушается эта цепочка, то страдает весь организм и это сказывается на состоянии здоровья человека. Впервые клиническая картина эндогенного гиперкортицизма была описана в 1912 г. Гарвеем Кушингом.
Гиперкотицизм проявляется тем, что кортизол в больших количествах замедляет выработку глюкозы, которая очень необходима нашим клеткам. В результате этого, функциональность многих клеток падает и наблюдается атрофирование тканей.
Патогенез
Основу болезни составляет нарушение обратной связи в функциональной системе гипоталамус-гипофиз – кора надпочечников, характеризующееся постоянно высокой активностью гипофиза и гиперплазией кортикотропов или, значительно чаще, развитием АКТГ- продуцирующих аденом гипофиза и гиперплазией коры обоих надпочечников.
В результате этого повышается скорость продукции и суммарная суточная экскреция практически всех фракций кортикостероидов с развитием симптомов гиперкортицизма. В основе синдрома Иценко-Кушинга лежит формирование автономной доброкачественной или злокачественной опухоли надпочечника или дисплазии надпочечника.
Синдром гиперкортицизма приводит к снижению либидо как у женщин, так и у мужчин. У последних он проявляется еще и импотенцией.
Причины
На сегодняшний день медикам не удалось до конца изучить причины, которые влияют на нарушение функции надпочечников. Известно лишь, что при любом факторе, который провоцирует повышение выработки гормонов надпочечниками, развивается заболевание. Провоцирующими факторами гиперкортицизма считаются:
- аденома, возникшая в гипофизе;
- образование опухолей в легких, поджелудочной, бронхиальном дереве, которые продуцируют АКТГ;
- длительный прием глюкокортикоидных гормонов;
- наследственный фактор.
Помимо вышеперечисленных факторов, на возникновение синдрома могут повлиять такие обстоятельства:
- травмирование или сотрясение мозга;
- черепно-мозговые травмы;
- воспаление паутинной оболочки спинного или головного мозга;
- воспалительный процесс в головном мозге;
- менингит;
- кровотечение в субарахноидальное пространство;
- повреждения центральной нервной системы.
Иногда признаки синдрома могут быть вызваны совсем другими факторами, но это только временное явление и не означает, что у человека истинный гиперкортицизм.
Частые причины развития псевдо – синдрома Кушинга – это ожирение, хроническая алкогольная интоксикация, беременность, стресс и депрессия, а иногда даже прием оральных контрацептивов, которые содержат смесь эстрогенов и прогестерона.
Повышение уровня кортизола в крови может произойти даже у грудных детей, когда в их организм вместе с грудным молоком поступает алкоголь.
Избыточный синтез глюкокортикоидов происходит под влиянием кортикотропина и кортиколиберина или независимо от них. В связи с этим выделяют АКТГ-зависимые и АКТГ-независимые формы патологии. К первой группе относятся:
- Центральный гиперкортицизм.
- АКТГ-эктопический синдром.
В медицине различают три вида гиперкортицизма, которые основываются на разнице причин возникновения патологии:
Во врачебной практике также встречаются случаи юношеского синдрома гиперкортицизма. Юношеский выделен в отдельный вид и обусловлен возрастными гормональными изменениями в организме подростка.
Экзогенный
Под влиянием внешних причин, таких как применение для лечения лекарственных средств, содержащих глюкокортикоиды может развиться ятрогенный или экзогенный гиперкортицизм. В основном он проходит после отмены провоцирующего патологию лекарства.
Эндогенный
Факторами развития эндогенного гиперкортицизма могут быть следующие причины:
- опухоли гипофиза (микроаденома гипофиза);
- бронхов;
- опухоли яичек, яичников;
- опухоль или гиперплазия коры надпочечников.
Провоцирующей опухолью бронхов или половых желез чаще всего бывает эктопированная кортикотропинома. Именно она вызывает повышенную секрецию кортикостероидного гормона.
Псевдо-синдром
Неистинный гиперкортицизм возникает по следующим причинам:
- алкоголизм;
- беременность;
- прием оральных контрацептивов;
- ожирение;
- стрессы или затяжные депрессии.
Наиболее часто причиной псевдо-синдрома становится сильное отравление организма алкоголем. При этом любые опухоли отсутствуют.
Симптомы гиперкортицизма у женщин и мужчин
Клиническая картина гиперкортицизма характеризуется симптомами:
- прогрессирующая слабость;
- постоянная утомляемость;
- бессонница;
- усталость;
- гипотония;
- психическая астения;
- отсутствие аппетита;
- тошнота;
- рвота;
- запоры,
- сменяющиеся поносами;
- боли в животе;
- снижение массы тела.
Патологическое увеличение показателя глюкокортикоидов приводит к появлению синдрома гиперкортицизма. Пациенты утверждают о жалобах, связанных с изменением внешности и сбоем функционирования сердечно-сосудистой системы, а также костно-мышечной, репродуктивной, нервной систем. Клинические проявления заболевания также вызваны повышенным содержанием альдостерона и андрогенов, вырабатываемых надпочечников.
Симптомы у женщин

Гиперкортицизм у женщин проявляется следующими симптомами:
- гирсутизмом;
- вирилизацией;
- гипертрихозом;
- сбоем менструальных циклов;
- аменореей и бесплодием.
Самым «популярным» проявлением гиперкортицизма со стороны опорно-двигательного аппарата является остеопороз (он обнаруживается у 90 % людей, страдающих синдромом). Данная патология имеет свойство прогрессировать: сначала она дает знать о себе болью в суставах и костях, а затем – переломами рук, ног и ребер. Если остеопорозом страдает ребенок, у него наблюдается отставание от сверстников в росте.
Признаки у мужчин

Мужской гиперкортицизм проявляется проблемами в половой системе: снижением потенции и либидо, атрофией яичек и гинекомастией. Так же, гиперкотицизм может проявить себя сбоями нервной и сердечно-сосудистой систем.
- психозы и стрессы;
- смена эйфорического состояния депрессией;
- заторможенность;
- суициидальные попытки.
Кожа у пациентов имеет характерный «мраморный» оттенок с хорошо заметным сосудистым рисунком, склонна к шелушению, сухости, перемежается с участками потливости. На коже плечевого пояса, молочных желез, живота, ягодиц и бедер образуются полосы растяжения кожи – стрии багровой или цианотичной окраски, длиной от нескольких миллиметров до 8 см и шириной до 2 см. Наблюдаются кожные высыпания (акне), подкожные кровоизлияния, сосудистые звездочки, гиперпигментация отдельных участков кожи.
Негативно сказывается синдром на гормональном фоне пациента, наблюдается нестабильное эмоциональное состояние: депрессия чередуется с эйфорией и психозом.
Осложнения
Одним из самых опасных осложнений гиперкортицизма является адренолиновый криз, который проявляется:
- нарушением сознания;
- рвотой и высоким давлением;
- гиперкалиемией;
- гипонатриемией;
- гипогликемией;
- болями в животе;
- метаболическим ацидозом.
Синдром Кушинга, который перешел в хроническую форму способен привести к гибели человека, поскольку провоцирует ряд тяжелых осложнений, а именно:
- декомпенсация сердца;
- инсульт;
- сепсис;
- пиелонефрит тяжелой степени;
- недостаточность почек хронической формы;
- остеопороз, при котором происходят многочисленные переломы позвоночника.
Диагностика
Для диагностики данного заболевания используют следующие методы:
- анализ крови на адренокортикотропный гормон и кортикостероиды;
- гормональные пробы мочи;
- рентген головы, костей скелета;
- МРТ или КТ головного мозга.
Диагноз ставится четко при наличии всех исследований. Его следует дифференцировать с сахарным диабетом и ожирением.

Ни один из лабораторных диагностических тестов на гипер-кортизолизм нельзя считать абсолютно надёжным, поэтому часто рекомендуют их повторять и комбинировать. Диагноз гиперкортицизма устанавливают на основании повышенной экскреции свободного кортизола с мочой или нарушенной регуляции гипоталамо-гипофизарно-надпочечниковой системы:
- суточная экскреция свободного кортизола и 17-гидроксикортикостерона повышена;
- суточный биоритм секреции кортизола отсутствует;
- содержание кортизола в 23—24 ч повышено.
Исследования в амбулаторных условиях
-
Свободный кортизол в суточной моче. Доля ложноотрицательных результатов в этом тесте достигает 5-10%, поэтому исследование рекомендуют проводить 2—3 раза. Ложноположительные результаты также провоцируют приём фенофибрата, карбамазепина и дигоксина, а ложноотрицательные результаты возможны при сниженной клубочковой фильтрации ( Если в обоих указанных выше тестах не подтверждается гиперкортизодизм, его наличие у больного маловероятно.
Лечение
На основании данных, полученных в ходе диагностики, врач может предложить один из трех методов лечения гиперкортицизма:
Лекарственные препараты
Препараты могут назначаться как самостоятельно, так и в составе комплексной терапии. Основу медикаментозного лечения гиперкортицизма составляют лекарственные средства, действие которых направлено на снижение выработки гормонов в надпочечниках. К подобным медикаментам относятся такие препараты, как Метирапон, Аминоглютетимид, Митотан либо Трилостан. Обычно их назначают при наличии противопоказаний к остальным методам лечения и в тех случаях, когда эти методы (например, оперативный) оказались неэффективными
Лучевая терапия
Лучевую терапию назначают в том случае, когда синдром спровоцирован аденомой гипофиза. В таком случае оказывается на пораженную область лучевое воздействие, что провоцирует понижение выработки адренокортикотропного гормона. Вместе с лучевой терапией применяется медикаментозное или хирургическое лечение. Таким образом, удается добиться максимально позитивного результата в лечении гиперкортицизма.
Хирургическое вмешательство
Гипофизный синдром Кушинга на поздних этапах нуждается в оперативной терапии. Больному назначают транссфеноидальную ревизию гипофиза и устраняют аденому посредством микрохирургической техники. Этот терапевтический метод приносит наибольший эффект и отмечается быстрым улучшением состояния после проведения операции. В тяжелых случаях при хирургическом вмешательстве больным удаляют два надпочечника. Таким пациентам показан пожизненный прием глюкокортикоидов.
От чего зависит эффективность лечения?
У гиперкортицизма может быть стремительное развитие, то есть все симптомы появляются в течении 6-12 месяцев и может быть постепенное развитие клинической картины в течении 3-10 лет. Лечение будет зависеть от правильной диагностики, от тяжести заболевания и от быстроты развития симптоматики. Лечение должно быть нацелено на устранение клинических проявлений и нормализацию уровня кортизола.
При средней и легкой степени тяжести применяются лекарственные препараты, которые не будут давать организму вырабатывать лишнее количество гормонов надпочечников или назначается лучевая терапия, которая снижает активность гипофиза. Если это всё не дает должного эффекта, то применяют хирургическое лечение. В процессе такого вмешательства опухоль гипофиза удаляют. Либо проводится адреналэктомия, то есть устранение одного из надпочечников, но после такой операции необходима постоянная заместительная терапия.
Прогноз синдрома
При игнорировании лечения синдрома гиперкортицизма развиваются необратимые изменения, приводящие к летальному исходу у 40-50% пациентов. Если причиной синдрома явилась доброкачественная кортикостерома, прогноз удовлетворительный, хотя функции здорового надпочечника восстанавливаются только у 80% пациентов. При диагностике злокачественных кортикостером прогноз пятилетней выживаемости – 20-25% (в среднем 14 месяцев). При хронической надпочечниковой недостаточности показана пожизненная заместительная терапия минерало- и глюкокортикоидами.
В целом прогноз определяется своевременностью диагностики и лечения, причинами, наличием и степенью выраженности осложнений, возможностью и эффективностью оперативного вмешательства. Пациенты с синдромом гиперкортицизма находятся на динамическом наблюдении у эндокринолога, им не рекомендуются тяжелые физические нагрузки, ночные смены на производстве.
Синдром Кушинга (СК) — это комплекс клинических симптомов, возникающих вследствие избытка ГКС. Субклиническая гиперкортизолемия, которую чаще всего диагностируют при исследованиях по поводу инциденталомы надпочечника — это состояние незначительного избытка ГКС, вызванное чрезмерной секрецией кортизола опухолью надпочечника, приводящее к торможению синтеза ГКС противоположным надпочечником, без характерных симптомов, но чаще всего возможны сахарный диабет, абдоминальное ожирение, артериальная гипертензия, сердечно-сосудистые события и остеопороз.
Классификация СК в зависимости от этиологии:
1. Эндогенный СК: вследствие чрезмерного синтеза ГКС надпочечниками:
1) АКТГ – независимый СК ( первичный гиперкортицизм):
а) автономные опухоли надпочечников — обычно одиночные, реже множественные аденомы; рак надпочечника →разд. 11.6. Опухоли, происходящие из пучковой зоны, секретируют в избытке исключительно кортизол, остальные типы опухолей (из сетчатой зоны или смешанные) — также и андрогены. Избыток кортизола ингибирует секрецию КРГ и АКТГ → происходит атрофия ткани коры пораженного надпочечника (расположенной за пределами капсулы опухоли), а также ткани коры второго надпочечника; нередко возникают множественные узлы коры надпочечника (описываемые как нодулярная гиперплазия), являющиеся поликлональными образованиями, в отличие от аденом, развивающихся из моноклонального источника.
б) макронодулярная гиперплазия надпочечников — причиной являются эктопические рецепторы в коре надпочечников, реагирующие на нетипичные стимулирующие раздражители, чаще всего на желудочный ингибиторный пептид (GIP), в настоящее время называемый глюкозозависимым инсулинотропным полипептидом, секретируется после еды в пищеварительном тракте; другие стимулирующие факторы — это катехоламины, вазопрессин, ТТГ, ЛГ, хорионический гонадотропин (ХГЧ), ФСГ, эстрогены в высокой концентрации, пролактин и интерлейкин 1;
в) микронодулярная гиперплазия надпочечников (первичная пигментированная микронодулярная гиперплазия [дисплазия] коры надпочечников) — генетически детерминированная семейная форма (синдром Карнея, с наличием других нарушений: миксом кожи, сердца и молочных желез, светло-коричневых пятен на коже, опухолей яичек, иногда других эндокринологических нарушений, напр. акромегалии) и спорадическая форма, при которой могут играть роль иммуноглобулины, провоцирующие гиперплазию коры надпочечников. Подобно другим АКТГ-независимым формам, ткань надпочечника между узелками может иметь атрофический характер.
2) АКТГ – зависимый СК ( вторичный гиперкортицизм) — гипофизарная форма (избыточный синтез АКТГ гипофизом, иначе говоря, болезнь Иценко-Кушинга →разд. 8.4.3; самая частая причина СК), синдром эктопической секреции АКТГ опухолью, локализированной вне гипофиза (значительно реже) или синдром эктопической секреции КРГ (реже всего).
2. Экзогенный СК: вызванный приёмом глюкокортикостероидных препаратов, в дозах, превышающих необходимые для заместительной терапии (наиболее частая причина СК), независимо от формы ЛС (таблетки, ингаляционные препараты, мази, растворы для инъекций, в т. ч. для внутрисуставных). наверх
КЛИНИЧЕСКАЯ КАРТИНА И ЕСТЕСТВЕННОЕ ТЕЧЕНИЕ наверхнаверх
1. Субъективные симптомы: изменение черт лица или фигуры тела, мышечная слабость и плохая переносимость физической нагрузки, склонность кожи к травматизации — тяжело заживающие язвы, склонность к возникновению гематом; полидипсия и полиурия (→ необходимо проконтролировать гликемию; в тяжёлых случаях может развиться гиперосмолярный гипергликемический синдром); повышенный аппетит; головная боль и головокружения (→ следует проконтролировать артериальное давление); эмоциональная лабильность, склонность к депрессии, ухудшение памяти, редко психотические состояния; боли в костях (в случае остеопороза → следует искать патологические переломы тел позвонков, ребер, лобковых и седалищных костей); склонность к инфекциям, особенно оппортунистическим (напр. грибковым), часто с тяжёлым течением, а также к туберкулезу; симптомы ишемической болезни сердца (→ выполнить контроль липидограммы), сердечной недостаточности или венозных тромбозов и тромбоэмболий (протромботическое действие ГКС), симптомы язвенной болезни желудка и двенадцатиперстной кишки (особенно у пациентов, принимающих НПВП); симптомы мочекаменной болезни (из-за гиперкальциурии и гиперфосфатурии); снижение потенции у мужчин, скудные менструации или вторичная аменорея у женщин.наверх
2. Объективные симптомы: ожирение центрального типа, с отложением жира на туловище и шее («бычья шея»), с наличием жировых подушек в надключичных ямках и с тонкими конечностями; лицо округлое («лунообразное лицо»), часто покрасневшее (вследствие гиперемии и истончения кожи), с расширенными сосудами; короткая толстая шея; атрофия мышц конечностей и туловища; широкие, красные или красно-синие растяжки на коже живота, бёдер, молочных желез, а у молодых лиц — также вокруг подмышечных, локтевых и подколенных ямок (→ следует дифференцировать с узкими, розовыми, множественными растяжками кожи, которые возникают у молодых лиц в период быстрого увеличения массы тела и со временем бледнеют); истончение кожи, легко возникающие кровоизлияния в кожу, иногда спонтанные петехии; симптомы гиперандрогенизации разной степени тяжести — угревые высыпания и гирсутизм (→ следует выполнить дифференциальную диагностику с синдромом поликистозных яичников); артериальная гипертензия (у большинства больных, в основном лёгкая или умеренная), гиперпигментация кожи (у пациентов с длительно существующей высокой концентрацией АКТГ); отеки на нижних конечностях.
3. Естественное течение: при субклиническом СК, даже длительном, развитие характерного комплекса симптомов может не произойти; риск прогрессирования в выраженную форму СК невысокий, поэтому субклинический СК не следует изначально рассматривать как раннюю фазу СК. Развернутый СК диагностируется только на поздней стадии длительно протекающей болезни . Значительно чаще присутствуют только некоторые симптомы, напр. нарушение толерантности к глюкозе или сахарный диабет, дислипидемия, артериальная гипертензия и быстрое увеличение массы тела (ожирение), составляющие картину метаболического синдрома; также повышается риск остеопороза.
СК следует подозревать и диагностировать в следующих ситуациях:
1) у пациентов с множественными и прогрессирующими симптомами гиперкортизолемии, в особенности с наиболее характерными (типичные растяжки, атрофия проксимальных групп мышц нижних конечностей и плечевых областей, гиперемия лица, легкое возникновение кровоподтёков);
2) у пациентов с атипичным течением артериальной гипертензии, сахарного диабета или остеопороза, что вызывает подозрение о их вторичном происхождении (особенно при резистентности к лечению или возникновение у лиц молодого возраста);
3) при случайном выявлении опухоли надпочечника (инциденталома).
При существенном клиническом подозрении на наличие СК единичного нормального результата любого скринингового анализа недостаточно для исключения заболевания. Всегда следует исключать предварительный приём ГКС пациентом (экзогенный СК).
Дополнительные методы исследования
1. Основные биохимические исследования: гипокалиемия и гиперкалиурия, гипергликемия (нарушение толерантности к глюкозе или сахарный диабет), повышенное содержание общего холестерина, ХС-ЛПНП и триглицеридов, снижение концентрации ХС-ЛПВП.
2. Общий анализ крови: эритроцитоз, лейкоцитоз и тромбоцитоз, повышенная концентрация гемоглобина, лимфоцитопения, эозинопения, моноцитопения.
3. Гормональные исследования гипоталамо-гипофизарно-надпочечниковой системы (границы норм могут отличаться — необходимо удостовериться, какие нормы приняты в лаборатории, проводящей анализ):
1) подтверждение гиперкортизолемии — исследования в случае подозрения на наличие СК →рис. 11.2-1:
а) отсутствие суточного ритма секреции кортизола — повышенная поздневечерняя (в 23:00–24:00) концентрация кортизола в сыворотке крови >149 нмоль/л (5,4 мкг/дл) или в слюне (>4,0 нмоль/л [145 нг/дл]); утренняя концентрация кортизола часто находится в пределах референтных значений;
б) повышенная экскреция свободного кортизола с мочой (с целью исключения необходимы 3 суточные порции мочи) — в 3–4 раза, превышающий верхнюю границу нормы результат (330 нмоль/24 ч [120 мкг/24 ч]);
в) недостаточное снижение концентрации кортизола в сыворотке крови при исполнении супрессивного теста с 1 мг дексаметазона (ночной супрессивный тест с дексаметазоном, короткий супрессивный тест с дексаметазоном): следует назначить пациенту приём 1 мг дексаметазона п/о перед сном (в 22:00–23:00) и определить концентрацию кортизола в сыворотке крови на следующий день утром между 8:00 и 9:00 натощак; или при 2-дневном супрессивном тесте с 2 мг дексаметазона следует назначить пациенту приём 0,5 мг дексаметазона п/о каждые 6 ч на протяжении 2-х суток и определить кортизолемию через 48 ч после приема первой дозы — концентрация поиск причины гиперкортизолемии — исследования, подтверждающие диагноз СК и определяющие его этиологию →рис. 11.2-2:
а) уровень АКТГ в сыворотке крови — зависит от этиологии СК: уровень АКТГ 4 пмоль/л (20 нг/л) — о АКТГ-зависимом СК (болезни Иценко-Кушинга — БИК); при значении 2–4 пмоль/л (10–20 нг/л) следует провести тест стимуляции с КРГ;
б) тест стимуляции с КРГ (тест стимуляции синтеза АКТГ и посредственно кортизола с помощью КРГ): при болезни Иценко-Кушинга характерным является многократное повышение концентрации АКТГ после стимуляции КРГ, но в случае значительно повышенных исходных значений существенным принято считать повышение уровня АКТГ на ≥35–50 % и кортизола на ≥14–20 %. При АКТГ-независимом СК ответ на КРГ обычно отсутствует либо незначителен.
в) тест ингибирования 8 мг дексаметазона (2 мг каждые 6 ч в течение 2 суток; в настоящее время выполняется реже) — результаты зависят от этиологии СК; его роль состоит в дифференциации между болезнью Иценко-Кушинга и автономными формами гиперкортицизма с избытком кортизола (гормонально активная опухоль надпочечника, синдром эктопического АКТГ и нодулярная гиперплазия надпочечников). При болезни Иценко-Кушинга выделение кортизола и его метаболитов обычно снижается на ≥50 %, при этом в случае автономной секреции кортизола ингибирование отсутствует. Результат теста является недостоверным, напр., в случае наличия рецепторов к глюкокортикоидам в опухоли, эктопически секретирующей АКТГ.
г) реактивность надпочечников на нетипичные стимулы — следует проверить в случае подозрения на макронодулярную гиперплазию надпочечников; необходимо определить уровень кортизола в сыворотке изначально и на 30, 60, 90 и 120 мин после завтрака или после пероральной нагрузки 75 г глюкозы; после принятия вертикального положения; после п/о приёма 10 мг метоклопрамида, после в/в введения 100 мкг ГнРГ или 200 мкг ТРГ; в пользу диагноза свидетельствует повышение уровня кортизола.
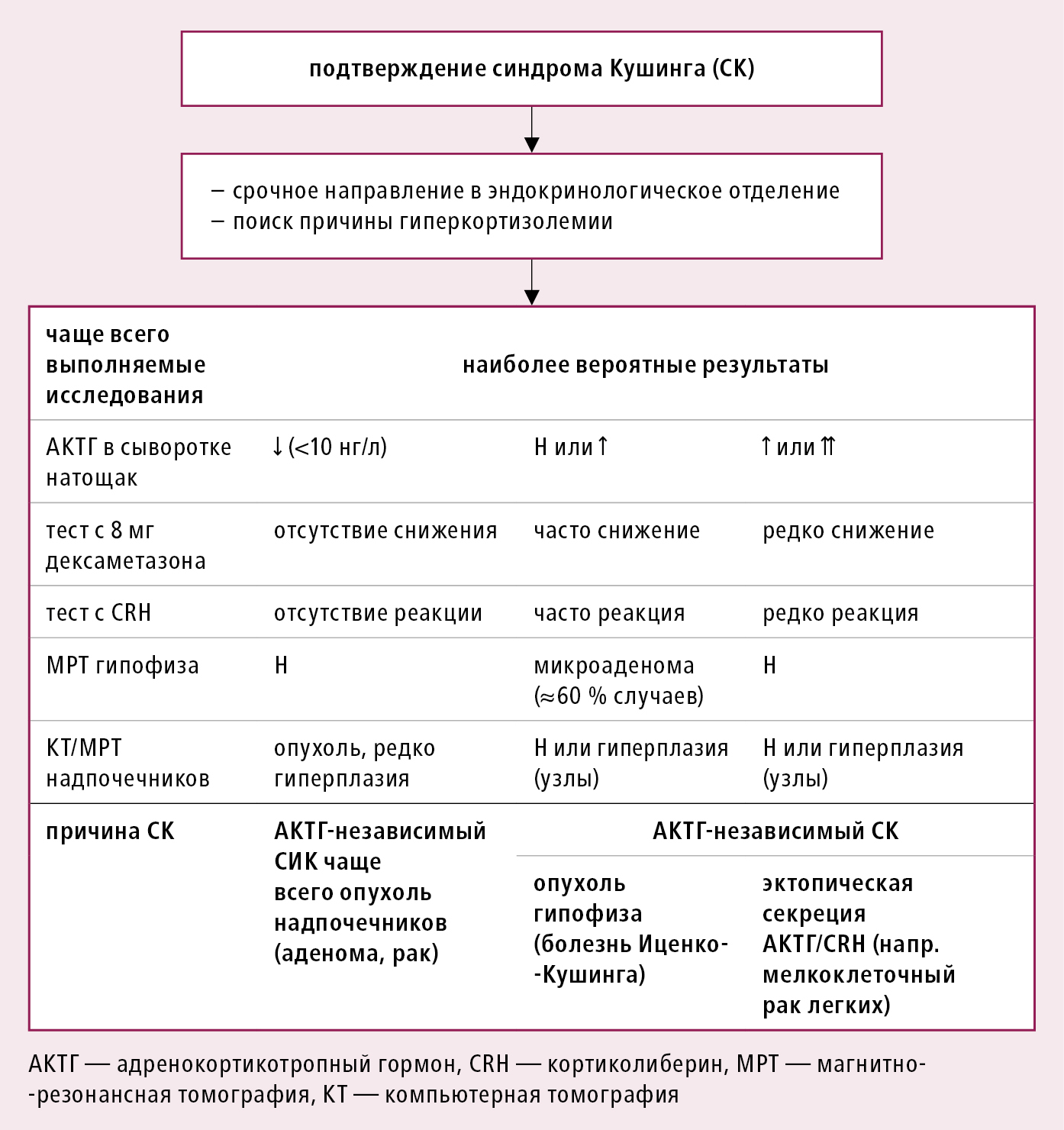
Рисунок 11.2-2. Алгоритм диагностики для определения этиологии синдрома Иценко-Кушинга
4. Визуализирующие исследования: МРТ гипофиза →разд. 8.4.3. КТ или, МРТ надпочечников — изменения, зависящие от причины СК →рис. 11.2-1:
1) автономная опухоль/опухоли коры надпочечников — при КТ односторонняя опухоль надпочечника, со свойствами аденомы →разд. 11.5; признаки атрофии другого надпочечника; реже множественные билатеральные аденомы коры надпочечников. При МРТ значительное содержание липидов, быстрое вымывание контрастного вещества. Гормонально активный рак надпочечника →разд. 11.6.
2) макронодулярная гиперплазия надпочечников — при КТ надпочечники симметричные, обычно увеличенные, часто с полициклическими контурами, а их плотность соответствует аденомам. МРТ обнаруживает в надпочечниках значительное содержание липидов.
3) микронодулярная гиперплазия надпочечников — при КТ и МРТ надпочечники симметричные, небольших или нормальных размеров; диагноз выставляется интраоперационно (характерная желто-черная окраска, вызванная присутствием липофусцина в узлах). РГ костей — признаки остеопороза, патологические переломы; в детском и юношеском возрасте часто отставание костного возраста. Денситометрия — признаки остеопении или остеопороза, особенно в поясничном отделе позвоночника и проксимальной части бедренной кости. Рецепторная сцинтиграфия с использованием аналогов соматостатина, с целью обнаружения нейроэндокринных опухолей, эктопически секретирующих АКТГ, или сцинтиграфия с йодхолестерином с целью выявления эктопически размещённой опухоли или идентификации автономно-секретирующей опухоли у пациентов с опухолями в обоих надпочечниках.
Диагностический алгоритм →рис. 11.2-1 и рис. 11.2-2. Как подтверждение, так и исключение гиперкортизолемии требует проведения ≥2 разных исследований.
1. Клинически выраженный СК: субъективные и объективные симптомы СК, гиперкортизолемия со сниженным уровнем АКТГ (надпочечниковая форма — АКТГ-независимый СК) или с повышенным уровнем АКТГ (аденома гипофиза или эктопическая секреция АКТГ или КРГ — АКТГ-зависимый СК); ответ в тесте с КРГ зависит от причин гиперкортизолемии; отсутствие ингибирования секреции кортизола (при опухоли надпочечника) или ингибирование только с помощью большой дозы [8 мг] дексаметазона (при аденоме гипофиза); иногда повышенный уровень андрогенов. Опухоль или опухоли надпочечников, обнаруженные при КТ/МРТ, или опухоль гипофиза при МРТ, либо, значительно реже, эктопический источник АКТГ или КРГ, обнаруженный методом рецепторной сцинтиграфии.
2. Субклиническая гиперкортизолемия, вызванная автономной опухолью или опухолями коры надпочечников (ранее — субклинический синдром Кушинга) вызывает много противоречий, поскольку критерии диагностики ещё не установлены. Необходимо оценить клиническую картину (обращая внимание на остеопению/остеопороз, абдоминальное ожирение, артериальную гипертензию, сахарный диабет) и следующие результаты дополнительных исследований (для постановки диагноза рекомендуется наличие 2-х или 3-х, и даже 4-х критериев):
1) тест с 1 мг дексаметазона — концентрация кортизола в сыворотке крови ≥94 нмоль/л (3,4 мкг/дл);
2) утренняя концентрация АКТГ в сыворотке верхней границы нормы;
4) концентрация кортизола в сыворотке крови в 23:00–24:00 ≥149 нмоль/л (5,4 мкг/дл).
Дифференциальная диагностика АКТГ зависимого и АКТГ независимого СК →рис. 11.2-2 .
Другие состояния с избытком ГКС:
1) синдром резистентности к ГКС — синдром частично нарушенной чувствительности ГКС рецептора (генетически обусловленный, редкий); повышенные концентрации АКТГ, кортизола, андрогенов и альдостерона в сыворотке крови, без симптомов избытка кортизола, с признаками андрогенизации у женщин и гиперальдостеронизма; сохранён суточный ритм секреции кортизола, а также ответ гипофиза и надпочечников на КРГ. Лечение: дексаметазон 1,0–1,5 мг/сут. с целью ингибирования секреции АКТГ.
2) функциональные синдромы (т. н. псевдо-СК), при которых обнаруженная гиперкортизолемия не является результатом органических изменений в пределах гипофизарно-надпочечниковой системы, но возникает вследствие других нарушений (гиперкортизолемия не требует лечения):
а) депрессия — гиперкортизолемия и нарушение ингибирования дексаметазоном, но сохранён суточный ритм секреции кортизола и нормальный уровень АКТГ;
б) беременность — в крови повышается уровень транскортина и, следовательно, кортизола. Синтез КРГ в плаценте возрастает в III триместре, увеличивается экскреция свободного кортизола с мочой; сохранён суточный ритм секреции кортизола.
в) алкоголизм — в немногих случаях наблюдаются соматические признаки СК (изменение метаболизма кортизола в печени и влияние алкоголя на ЦНС); абстиненция вызывает исчезновение симптомов;
г) психическая анорексия — повышенный уровень кортизола, в основном в результате снижения почечного клиренса, но возможен также повышенный синтез АКТГ. Нарушение ингибирования дексаметазоном является признаком приобретённой резистентности ГКС рецептора, что также объясняет отсутствие каких-либо признаков гиперфункции коры надпочечников.
Лечение осложнений СК: артериальной гипертензии, нарушений углеводного и липидного обмена, остеопороза, психических нарушений. Некоторые осложнения исчезают после успешного этиологического лечения СК. наверх
Зависит от этиологии СК; является крайне необходимым при манифестирующем СК и при наличии осложнений гиперкортизолемии. Вариантом выбора является оперативное лечение, вид которого зависит от причины СК (удаление аденомы гипофиза при болезни Иценко-Кушинга, опухоли надпочечника или — значительно реже — опухолевой ткани, эктопически секретирующей АКТГ), в то же время следует удержаться от терапевтических назначений, если диагноз СК сомнителен. Рекомендации The Endocrine Society (2015) советуют не начинать лечения в случае получения пограничных результатов гормональных исследований, если типичные клинические проявления СК отсутствуют.
1. Аденома гипофиза →разд. 8.4.3.
2. Автономная опухоль/опухоли коры надпочечников: методом выбора является хирургическое удаление опухоли надпочечника, после предоперационной подготовки ингибитором стероидогенеза → используется кетоконазол 400–800 мг/сут в 3 приёма (редко до 1200 мг/сут); сначала достигается биохимическая ремиссия, а по истечении ≈3 нед. — клиническое улучшение; следует проявлять осторожность, чтобы не спровоцировать дефицита ГКС и симптомов тяжелого криза острой надпочечниковой недостаточности (некоторые опухоли проявляют крайне высокую чувствительность к ингибиторам синтеза кортизола). Альтернативное лечение: метирапон — дозировка подбирается индивидуально, в зависимости от выраженности гиперкортизолемии и переносимости препарата, начально 250–750 мг/сут, у пациентов с тяжёлым СК — даже 1500 мг/сут (в специализированных центрах); реже применяют аминоглутетимид 500-750 мг/сут. Митотан (обычно ≈3 г/сут) используется при раке надпочечника, а этомидат — является единственным препаратом для в/в применения. Профилактика кортикостероидами при вмешательствах — как и в случае операции у больных с гипокортицизмом →см. выше. Первым критерием ремиссии первичного гиперкортицизма после оперативного лечения является утренняя концентрация кортизола 3. Макронодулярная и микронодулярная гиперплазия надпочечников: методом выбора считается билатеральная адреналэктомия; прикрытие гидрокортизоном — как при аденомэктомии.
В случаях длительного течения СК (независимо от этиологии) могут возникать сосудистые осложнения вследствие артериальной гипертензии. При наличии нелеченого СК даже лёгкой степени тяжести — смертность повышается в 4 раза (преимущественно по причине сердечно-сосудистых заболеваний и инфекций) по сравнению с общей популяцией. После эффективного оперативного лечения многие из проявлений СК, в т. ч. артериальная гипертензия и сахарный диабет, исчезают или ослабевают на протяжении 12 мес. Повышенный риск летального исхода по причине сердечно-сосудистых заболеваний сохраняется в течение ≈5 лет. наверх
1. Удаление аденомы/аденом коры надпочечников приводит к полному исчезновению симптомов СК. Рецидив опухоли происходит из-за повторного роста образования из фрагментов коры надпочечника, оставшихся в жировой ткани, в то же время рецидив радикально удаленной аденомы не возможен. Может быть необходимым периодическое заместительное лечение.
2. Билатеральная адреналэктомия при макронодулярной и микронодулярной гиперплазии надпочечников вызывает исчезновение симптомов СК, однако необходима постоянная заместительная терапия. При синдроме Карнея прогноз зависит от вида сопутствующих изменений.
3. При раке коры надпочечников (→см. ниже) прогноз зависит от степени распространенности опухоли и объёма хирургического лечения. У пациентов после билатеральной адреналэктомии обязательна постоянная заместительная терапия.
- chevron_rightСервисы
- Сообщество пациентов «Дом ЭКО»
- Рассчитать месяц беременности
- Календарь овуляции
- Календарь менструального цикла
- Самодиагностика
- Календарь сдачи анализов
- Калькулятор стоимость анализов
- Рассчитать срок беременности
- Рассчитать дату родов
- Рассчитать дату родов после ЭКО
- Рассчитать эффективность ЭКО
- Калькулятор ХГЧ после ЭКО
- Расшифровка спермограммы
Лечением данного заболевания занимаются Эндокринологи.
Гиперкортицизм — нозология, являющаяся следствием нарушения работы гипоталамо-гипофизарно-надпочечниковой системы. В результате сбоя усиливается выработка глюкокортикостероидов — гормонов надпочечников, и формируется характерная клиническая картина заболевания.

Общая информация
Клиническая картина заболевания была описана одновременно двумя учеными — Николаем Иценко и Харви Кушингом, благодаря чему патология получила название «болезнь, или синдром, Иценко-–Кушинга».
Гиперкортицизм — широкое понятие, в которое входит комплекс различных состояний. Наиболее распространенными являются болезнь и синдром Иценко-–Кушинга. В первом случае патология обусловлена нарушениями в гипоталамо-гипофизарной системе. Чаще всего это аденома гипофиза — небольшая, доброкачественная опухоль, продуцирующая адренокортикотропный гормон. Во втором — изменения касаются непосредственно надпочечников. Чаще всего это аденомы и аденокарциномы.
В 1–2% случаев нозология провоцируется АКТГ-эктопированным синдромом — гормонально активной опухолью, локализованной в легких, тимусе, яичниках и яичках, железах внутренней секреции, поджелудочной и предстательной железе.
Лекарственная гиперкортицизм — патология, вызваная неправильным или нецелесообразным назначением кортикотропных гормонов.
Механизм развития болезни
В основе развития гиперкортицизма лежит повышенная секреция кортизола. Данный гормон провоцирует распад белков костей, мышц, кожи и внутренних органов. Со временем это приводит к дистрофии и атрофии тканей. Усиленная выработка глюкозы приводит к развитию стероидной формы диабета. Нарушение жирового обмена сопровождается характерным отложением жира в определенных зонах. Избыточная концентрация кортизола влияет и на почки. Как результат — в плазме крови повышается уровень натрия и снижается концентрация калия. Такие пациенты страдают от повышенного артериального давления, а в мышечной ткани усиливаются дистрофические процессы.
Сильнее всего при гиперкортицизме страдает миокард. Внешне это проявляется нарушением сердечного ритма, сердечной недостаточностью, кардиомиопатией.
Кроме того, кортизол угнетающе действует на иммунную систему. В результате пациенты становятся очень чувствительными к различного вида инфекциям.
Клиническая картина
Наиболее типичный симптом гиперкортицизма — ожирение. Этот признак выявляют у более чем 90% больных. Как правило, жир откладывается на лице, животе и спине. Конечности при этом остаются относительно худыми. Такое ожирение называют кушингоидным.
Лицо пациента по форме становится лунообразным, красного цвета с синюшным оттенком. Жир, отложенный в области седьмого шейного позвонка, создает так называемый бычий горб. Кожа тыльной стороны ладони становится истонченной, почти прозрачной.
Из-за атрофических процессов в мышцах развивается дисгормональная миопатия. Пациенты жалуются на снижение силы мышц, мышечную слабость, боль в мышцах. Характерными признаками болезни являются так называемые скошенные ягодицы и лягушачий живот, обусловленные гипотрофией мышц живота, бедер и ягодиц.

Кожа больных имеет специфический так называемый мраморный оттенок, склонна к шелушению и сухости. Сосудистый рисунок хорошо заметен. На плечах, в области груди, живота, ягодиц и бедер образуются багровые стрии — растяжки. Средняя их длина — 8 см, ширина — до 2 см. Отдельные участки кожи гиперпигментированы, наблюдаются акне, подкожные кровоизлияния.
Остеопороз — также частый симптом при гиперкортицизме. Костная ткань истончается, становится менее плотной, что приводит к сильному болевому синдрому, патологическим переломам, искривлению позвоночника. Из-за деформации позвоночного столба и сдавливания позвонков пациенты становятся сутулыми и ниже ростом.
Со стороны сердечной мышцы чаще всего наблюдается экстрасистолии, артериальная гипертензия, фибрилляция предсердий. Из-за атрофических процессов в миокарде развивается сердечная недостаточность. Это довольно серьезные нарушения, способные привести к летальному исходу.
При синдроме Иценко-–Кушинга страдает и центральная нервная система. Пациенты страдают от депрессии, стероидных психозов, делают попытки суицида.
Примерно у каждого десятого больного синдромом Иценко-–Кушинга развивается сахарный диабет, связанный с атрофическими процессами в поджелудочной железе. Характерная черта такого диабета — легкое течение. Длительное время у больных наблюдается нормальный уровень инсулина, а сама болезнь хорошо компенсируется диетой и препаратами, снижающими уровень сахара в крови.
У женщин может развиваться гиперандрогения — синдром, вызванный повышенным содержанием мужских половых гормонов. Она характеризуется нарушением менструального цикла, бесплодием, формирование вторичных половых признаков по мужскому типу.
Диагностика
Первое, что нужно сделать при появлении у больного признаков гиперкортицизма — подтвердить или опровергнуть повышенную продукцию кортизола надпочечниками. Для этого используют малую дексаметазоновую пробу.
Чаще всего ее выполняют по такому алгоритму:
- утром первого дня пациенту определяют уровень кортизола в сыворотке крови;
- в этот же день, в 24.00 больной принимает 1 мг дексаметазона внутрь;
- повторная проверка концентрации кортизола в сыворотке крови больного (утром следующего дня).
У здоровых лиц уровень кортизола снижается более чем в два раза, чего не происходит при гиперкортицизме.
Большая дексаметазоновая проба проводится в тех случаях, когда при малой не зафиксировалось должного подавления уровня кортизола, а также при необходимости провести дифференциальную диагностику между болезнью Иценко-–Кушинга и кортикостеромой, а также АКТГ-синдромом.
Способ проведения большой дексаметазоновой пробы отличается от малой только дозировкой препарата — вместо 1 мг больному советуют принять 8 мг препарата. При болезни Иценко-–Кушинга введения лекарства провоцирует снижение концентрации кортизола в сыворотке плазмы на 50%. При кортикостероме или АКТГ-синдроме показатель остается прежним. Это объясняется особенностями работы гипоталамуса и гипофиза.
Для выявления аденомы гипофиза проводят МРТ головного мозга. Кроме того, при подозрении на патологию показано КТ или МРТ надпочечников — на патологию указывает их двусторонняя гиперплазия. Эти же методы применяются для визуализации кортикостеромы, расположенной во внутренних органах.
Для диагностики осложнений болезни показаны биохимические исследования, рентгенография позвоночника и другие методики. Объем исследований определяется индивидуально, в зависимости от состояния пациента.
Лечение
Для лечения болезни применяются как консервативные, так и оперативные методы. Прежде всего, пациенту назначают средства, угнетающие синтез стероидов. Они эффективны при эндогенном характере заболевания.
Если при проведении магнитно-резонансной томографии удается четко визуализировать аденому гипофиза, показано ее оперативное удаление. В таком случае устойчивая ремиссия развивается у девяти из десяти больных. Если аденома не просматривается, пациенту рекомендуют протонотерапию на область гипофиза.
Основной метод лечение кортикостеромы — адреналэктомия. Иногда, особенно при тяжелом протекании болезни, проводится одностороннее удаление надпочечника. Это позволяет уменьшить выраженность симптомов заболевания.
Особую роль при данной патологии играет симптоматическое лечение. Как правило, больным рекомендуют лекарственные средства, снижающие АД, сахароснижающие, и медикаменты, предназначенные для терапии остеопороза. Для нормализации электролитного обмена назначают препараты калия.
Прогноз и профилактика
Прогноз при синдроме Иценко-–Кушинга зависит от таких факторов:
- своевременность диагностики и начала лечения;
- возраста пациента;
- индивидуальной реакции на терапию;
- первопричины заболевания.
При отсутствии адекватной терапии или неправильном лечении показатель смертности в первые пять лет с момента диагностики заболевания достигает 50%. Наиболее высока вероятность хорошего клинического исхода при кортикостероме, несмотря на то, что функция второго надпочечника восстанавливается только у восьми из 10 пациентов.
При злокачественной кортикостероме средний коэффициент пятилетней выживаемости не превышает 25%. Средняя продолжительность жизни при отсутствии лечения — один год и два месяца. Своевременная диагностика и ранее лечение значительно улучшают прогноз для жизни и здоровья больного.

